六一遇端午,北測陪你一起“粽”享歡樂

裝修板材
搜索
取消
清空記錄
歷史記錄
清空記錄
歷史記錄

口罩檢測報告
產品詳情
口罩檢測報告介紹
口罩檢測報告分多種,有國家標準的檢測報告、國際標準的檢測報告和按照行業標準測試的報告。不同產品和國家地區要求的標準有不同,口罩在國內常見的有GB2626-2019、GB19083-2010、GB/T32610-2016等標準。口罩檢測報告對口罩的功能、性能、外觀等按照對應標準進行測試,口罩檢測報告可用來證明口罩是否合格。實驗室獲得中國合格評定國家認可委員會CNAS認可后,可以在檢測報告上簽發CNAS蓋章。

CMA章是中國計量認證可用于產品質量評價、成果及司法鑒定,具有法律效力,CMA在通過認定的范圍內,可提供公正數據,國內通用。
口罩檢測涉及標準
下圖為國內常見的口罩檢測標準
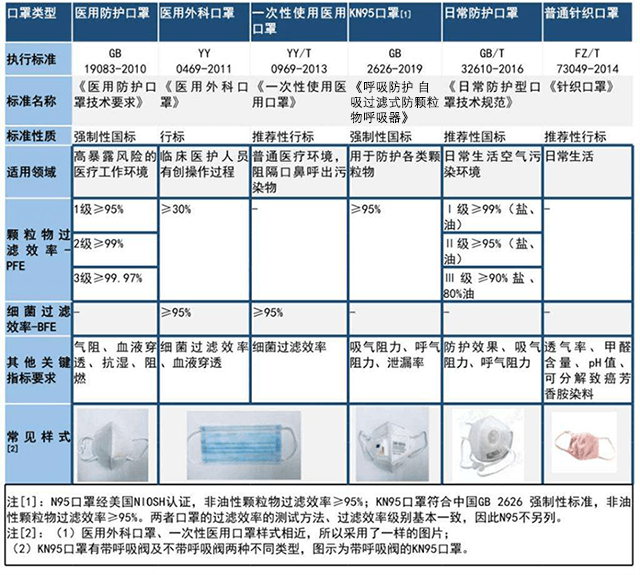
歐盟醫用口罩標準為EN14683-2019+AC-2019,歐盟防護口罩標準為EN149:2001+A1:2009。
辦理流程
1、檢測機構工程師確定產品信息,確定檢測項目及費用、周期問題;
2、填寫申請表;
3、安排口罩送樣
4、NTEK實驗室收到口罩樣品后安排檢測
5、草稿報告確認
2、填寫申請表;
3、安排口罩送樣
4、NTEK實驗室收到口罩樣品后安排檢測
5、草稿報告確認
6、確認信息無誤后出正式報告
口罩檢測報告模板
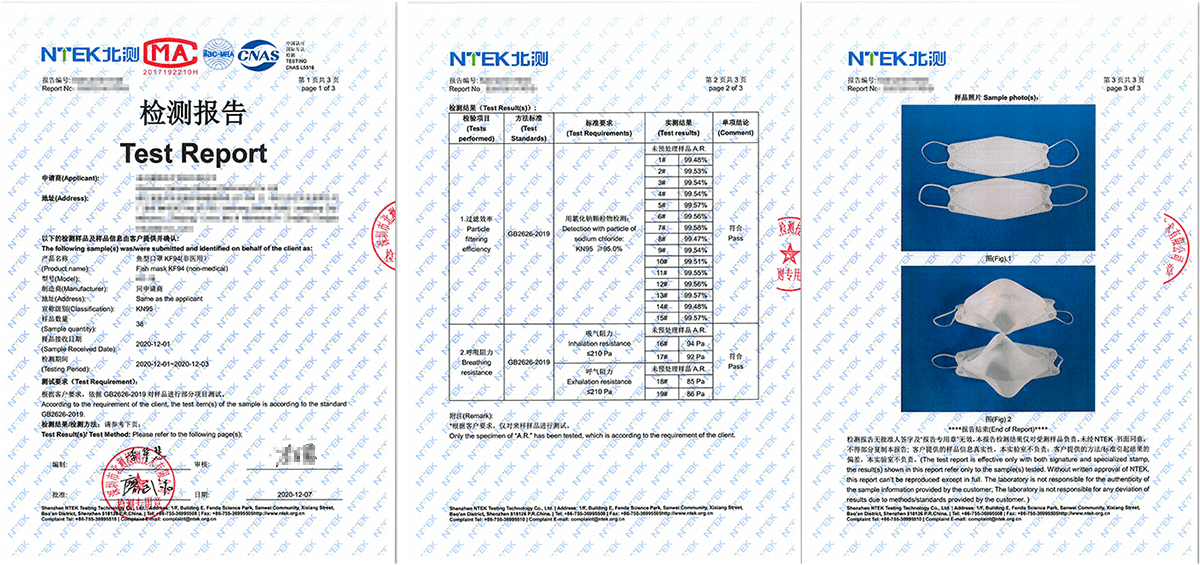
口罩標準及測試項目
| 序號 | 標準名稱 | 檢測標準 | 項目名稱 | 樣品數量 | 周期 |
| 1 | 醫用防護口罩技術要求 | GB19083-2010 | 口罩基本要求 | 80個+12包 | 5-8天 |
| 鼻夾 | |||||
| 口罩帶 | |||||
| 過濾效率 | |||||
| 氣流阻力 | |||||
| 合成血液穿透 | |||||
| 表面抗濕性 | |||||
| 微生物指標 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 阻燃性能 | |||||
| 皮膚刺激 | |||||
| 密合性 | |||||
| 2 | 醫用外科口罩 | YY 0469-2011 | 外觀 | 80+12包 | 5-8天 |
| 結構與尺寸 | |||||
| 鼻夾 | |||||
| 口罩帶 | |||||
| 合成血液穿透 | |||||
| 細菌過濾效率 | |||||
| 顆粒物過濾效率 | |||||
| 壓力差 | |||||
| 阻燃性能 | |||||
| 微生物 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 標志 | |||||
| 包裝 | |||||
| 皮膚刺激 | |||||
| 細胞毒性 | |||||
| 遲發超敏反應 | |||||
| 3 | 醫用外科口罩 | YY 0469-2011 | 外觀 | 80+12包 | 5-8天 |
| 結構與尺寸 | |||||
| 鼻夾 | |||||
| 口罩帶 | |||||
| 合成血液穿透 | |||||
| 細菌過濾效率 | |||||
| 顆粒物過濾效率 | |||||
| 壓力差 | |||||
| 阻燃性能 | |||||
| 微生物 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 標志 | |||||
| 包裝 | |||||
| 皮膚刺激 | |||||
| 細胞毒性 | |||||
| 遲發超敏反應 | |||||
| 4 | 一次性使用醫用口罩 | YY/T 0969-2013 | 外觀 | 60+12包 | 5-8天 |
| 結構與尺寸 | |||||
| 鼻夾 | |||||
| 口罩帶 | |||||
| 細菌過濾效率 | |||||
| 通氣阻力 | |||||
| 微生物 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 細胞毒性 | |||||
| 皮膚刺激 | |||||
| 遲發超敏反應 | |||||
| 5 | 呼吸防護用品 自吸過濾式防顆粒物呼吸器 | GB2626-2006 | 一般要求 | 80 | 7-12天 |
| 外觀檢查 | |||||
| 過濾效率(NaCl或石蠟油) | |||||
| 泄漏性 | |||||
| 呼吸阻力 | |||||
| 死腔 | |||||
| 視野 | |||||
| 頭帶 | |||||
| 可燃性 | |||||
| 連接和連接部件 | |||||
| 標識 | |||||
| 制造商提供的信息 | |||||
| 6 | 呼吸防護用品 自吸過濾式防顆粒物呼吸器 | GB2626-2019 | 基本要求 | 80 | 7-10天 |
| 外觀檢查 | |||||
| 過濾效率(NaCl或石蠟油) | |||||
| 泄漏性 | |||||
| 呼吸阻力 | |||||
| 死腔 | |||||
| 視野 | |||||
| 頭帶 | |||||
| 可燃性 | |||||
| 連接和連接部件 | |||||
| 清洗和消毒 | |||||
| 包裝 | |||||
| 標識 | |||||
| 制造商提供的信息 | |||||
| 實用性能 | |||||
| 7 | 日常防護型口罩技術規范 | GB/T32610-2016 | 基本要求 | 80+12包 | 7-10天 |
| 外觀要求 | |||||
| 耐摩擦色牢度(干/濕) | |||||
| 甲醛含量 | |||||
| pH值 | |||||
| 可分解致癌芳香胺染料 | |||||
| 環氧乙烷殘留量 | |||||
| 吸氣阻力 | |||||
| 呼氣阻力 | |||||
| 口罩帶及口罩帶與口罩體的連接處斷裂強力 | |||||
| 微生物指標 | |||||
| 下方視野 | |||||
| NaCl顆粒物過濾效率 | |||||
| 油性顆粒物過濾效率 | |||||
| 防護效果 | |||||
| 8 | 呼吸防護用品 自吸過濾式防顆粒物呼吸器 | EN149:2001+A1:2009 | 外觀檢查 | 120 | 7-12天 |
| 材料 | |||||
| Nacl穿透率 | |||||
| 油性穿透率 | |||||
| 死腔 | |||||
| 視野 | |||||
| 頭帶 | |||||
| 可燃性 | |||||
| 實用性能 | |||||
| 總泄漏率 | |||||
| 皮膚適應性 | |||||
| 呼吸阻力 | |||||
| 可拆卸部件 | |||||
| 呼氣閥 | |||||
| 部件接觸面 | |||||
| 制造商提供的信息 | |||||
| 阻塞 | |||||
| 包裝 | |||||
| 9 | 醫用外科口罩 | EN 14683:2005 | 一般要求 | 90 | 5-10天 |
| 細菌過濾效率 | |||||
| 壓力差 | |||||
| 抗合成血液穿透 | |||||
| 材料和結構 | |||||
| 微生物清潔度 | |||||
| 生物相容性 | |||||
| 10 | 醫用外科口罩 | EN 14683:2019 | 一般要求 | 130 | 5-10天 |
| 細菌過濾效率 | |||||
| 壓力差 | |||||
| 抗合成血液穿透 | |||||
| 微生物清潔度 | |||||
| 材料和結構 | |||||
| 生物相容性 | |||||
| 11 | 兒童口罩技術規范 | GB/T 38880-2020 | pH值 | 66+12包 | 10-15天 |
| 包裝 | |||||
| 口罩帶及口罩帶與口罩體的連接處斷裂強力 | |||||
| 可分解致癌芳香胺染料 | |||||
| 吸氣阻力 | |||||
| 呼氣阻力 | |||||
| 基本要求 | |||||
| 外觀質量要求 | |||||
| 安全警示 | |||||
| 尖端和邊緣銳利性 | |||||
| 微生物指標 | |||||
| 標識 | |||||
| 環氧乙烷殘留量 | |||||
| 甲醛含量 | |||||
| 細菌過濾效率 | |||||
| 耐干摩擦色牢度 | |||||
| 通氣阻力 | |||||
| 阻燃性能 | |||||
| 顆粒物過濾效率 | |||||
| 鼻夾耐折性 | |||||
| 鼻夾長度 | |||||
| 可遷移性熒光增白物 | |||||
| 防護效果 | |||||
| 呼吸閥蓋牢度 |
口罩檢測報告
產品詳情
口罩檢測報告介紹
口罩檢測報告分多種,有國家標準的檢測報告、國際標準的檢測報告和按照行業標準測試的報告。不同產品和國家地區要求的標準有不同,口罩在國內常見的有GB2626-2019、GB19083-2010、GB/T32610-2016等標準。口罩檢測報告對口罩的功能、性能、外觀等按照對應標準進行測試,口罩檢測報告可用來證明口罩是否合格。實驗室獲得中國合格評定國家認可委員會CNAS認可后,可以在檢測報告上簽發CNAS蓋章。

CMA章是中國計量認證可用于產品質量評價、成果及司法鑒定,具有法律效力,CMA在通過認定的范圍內,可提供公正數據,國內通用。
口罩檢測涉及標準
下圖為國內常見的口罩檢測標準

歐盟醫用口罩標準為EN14683-2019+AC-2019,歐盟防護口罩標準為EN149:2001+A1:2009。
辦理流程
1、檢測機構工程師確定產品信息,確定檢測項目及費用、周期問題;
2、填寫申請表;
3、安排口罩送樣
4、NTEK實驗室收到口罩樣品后安排檢測
5、草稿報告確認
2、填寫申請表;
3、安排口罩送樣
4、NTEK實驗室收到口罩樣品后安排檢測
5、草稿報告確認
6、確認信息無誤后出正式報告
口罩檢測報告模板

口罩標準及測試項目
| 序號 | 標準名稱 | 檢測標準 | 項目名稱 | 樣品數量 | 周期 |
| 1 | 醫用防護口罩技術要求 | GB19083-2010 | 口罩基本要求 | 80個+12包 | 5-8天 |
| 鼻夾 | |||||
| 口罩帶 | |||||
| 過濾效率 | |||||
| 氣流阻力 | |||||
| 合成血液穿透 | |||||
| 表面抗濕性 | |||||
| 微生物指標 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 阻燃性能 | |||||
| 皮膚刺激 | |||||
| 密合性 | |||||
| 2 | 醫用外科口罩 | YY 0469-2011 | 外觀 | 80+12包 | 5-8天 |
| 結構與尺寸 | |||||
| 鼻夾 | |||||
| 口罩帶 | |||||
| 合成血液穿透 | |||||
| 細菌過濾效率 | |||||
| 顆粒物過濾效率 | |||||
| 壓力差 | |||||
| 阻燃性能 | |||||
| 微生物 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 標志 | |||||
| 包裝 | |||||
| 皮膚刺激 | |||||
| 細胞毒性 | |||||
| 遲發超敏反應 | |||||
| 3 | 醫用外科口罩 | YY 0469-2011 | 外觀 | 80+12包 | 5-8天 |
| 結構與尺寸 | |||||
| 鼻夾 | |||||
| 口罩帶 | |||||
| 合成血液穿透 | |||||
| 細菌過濾效率 | |||||
| 顆粒物過濾效率 | |||||
| 壓力差 | |||||
| 阻燃性能 | |||||
| 微生物 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 標志 | |||||
| 包裝 | |||||
| 皮膚刺激 | |||||
| 細胞毒性 | |||||
| 遲發超敏反應 | |||||
| 4 | 一次性使用醫用口罩 | YY/T 0969-2013 | 外觀 | 60+12包 | 5-8天 |
| 結構與尺寸 | |||||
| 鼻夾 | |||||
| 口罩帶 | |||||
| 細菌過濾效率 | |||||
| 通氣阻力 | |||||
| 微生物 | |||||
| 無菌試驗 | |||||
| 環氧乙烷殘留量 | |||||
| 細胞毒性 | |||||
| 皮膚刺激 | |||||
| 遲發超敏反應 | |||||
| 5 | 呼吸防護用品 自吸過濾式防顆粒物呼吸器 | GB2626-2006 | 一般要求 | 80 | 7-12天 |
| 外觀檢查 | |||||
| 過濾效率(NaCl或石蠟油) | |||||
| 泄漏性 | |||||
| 呼吸阻力 | |||||
| 死腔 | |||||
| 視野 | |||||
| 頭帶 | |||||
| 可燃性 | |||||
| 連接和連接部件 | |||||
| 標識 | |||||
| 制造商提供的信息 | |||||
| 6 | 呼吸防護用品 自吸過濾式防顆粒物呼吸器 | GB2626-2019 | 基本要求 | 80 | 7-10天 |
| 外觀檢查 | |||||
| 過濾效率(NaCl或石蠟油) | |||||
| 泄漏性 | |||||
| 呼吸阻力 | |||||
| 死腔 | |||||
| 視野 | |||||
| 頭帶 | |||||
| 可燃性 | |||||
| 連接和連接部件 | |||||
| 清洗和消毒 | |||||
| 包裝 | |||||
| 標識 | |||||
| 制造商提供的信息 | |||||
| 實用性能 | |||||
| 7 | 日常防護型口罩技術規范 | GB/T32610-2016 | 基本要求 | 80+12包 | 7-10天 |
| 外觀要求 | |||||
| 耐摩擦色牢度(干/濕) | |||||
| 甲醛含量 | |||||
| pH值 | |||||
| 可分解致癌芳香胺染料 | |||||
| 環氧乙烷殘留量 | |||||
| 吸氣阻力 | |||||
| 呼氣阻力 | |||||
| 口罩帶及口罩帶與口罩體的連接處斷裂強力 | |||||
| 微生物指標 | |||||
| 下方視野 | |||||
| NaCl顆粒物過濾效率 | |||||
| 油性顆粒物過濾效率 | |||||
| 防護效果 | |||||
| 8 | 呼吸防護用品 自吸過濾式防顆粒物呼吸器 | EN149:2001+A1:2009 | 外觀檢查 | 120 | 7-12天 |
| 材料 | |||||
| Nacl穿透率 | |||||
| 油性穿透率 | |||||
| 死腔 | |||||
| 視野 | |||||
| 頭帶 | |||||
| 可燃性 | |||||
| 實用性能 | |||||
| 總泄漏率 | |||||
| 皮膚適應性 | |||||
| 呼吸阻力 | |||||
| 可拆卸部件 | |||||
| 呼氣閥 | |||||
| 部件接觸面 | |||||
| 制造商提供的信息 | |||||
| 阻塞 | |||||
| 包裝 | |||||
| 9 | 醫用外科口罩 | EN 14683:2005 | 一般要求 | 90 | 5-10天 |
| 細菌過濾效率 | |||||
| 壓力差 | |||||
| 抗合成血液穿透 | |||||
| 材料和結構 | |||||
| 微生物清潔度 | |||||
| 生物相容性 | |||||
| 10 | 醫用外科口罩 | EN 14683:2019 | 一般要求 | 130 | 5-10天 |
| 細菌過濾效率 | |||||
| 壓力差 | |||||
| 抗合成血液穿透 | |||||
| 微生物清潔度 | |||||
| 材料和結構 | |||||
| 生物相容性 | |||||
| 11 | 兒童口罩技術規范 | GB/T 38880-2020 | pH值 | 66+12包 | 10-15天 |
| 包裝 | |||||
| 口罩帶及口罩帶與口罩體的連接處斷裂強力 | |||||
| 可分解致癌芳香胺染料 | |||||
| 吸氣阻力 | |||||
| 呼氣阻力 | |||||
| 基本要求 | |||||
| 外觀質量要求 | |||||
| 安全警示 | |||||
| 尖端和邊緣銳利性 | |||||
| 微生物指標 | |||||
| 標識 | |||||
| 環氧乙烷殘留量 | |||||
| 甲醛含量 | |||||
| 細菌過濾效率 | |||||
| 耐干摩擦色牢度 | |||||
| 通氣阻力 | |||||
| 阻燃性能 | |||||
| 顆粒物過濾效率 | |||||
| 鼻夾耐折性 | |||||
| 鼻夾長度 | |||||
| 可遷移性熒光增白物 | |||||
| 防護效果 | |||||
| 呼吸閥蓋牢度 |
立即咨詢
獲取報價

選擇區號


 瀏覽器自帶分享功能也很好用哦~
瀏覽器自帶分享功能也很好用哦~